解放軍總醫院醫療保障中心藥劑科 西娜
經歷過去年年底新冠病毒“浪潮”般的洗禮,很多家長可能依然心有余悸,不愿孩子再受到病毒的侵襲,但現實往往不遂人愿,隨著新一波季節性流感的到來,“囤藥”之風再度刮起,我們能否通過抗病毒藥物來預防孩子們感染流感病毒,成為人們熱議的話題,今天我們就來幫您梳理一下。
流行性感冒(簡稱流感)是一種急性呼吸道疾病,由甲型或乙型流感病毒引起,偶爾由丙型流感病毒引起。全世界每年都有流感暴發。在身體健康的兒童中,流感通常是急性、自限性且無并發癥的疾病,但也可導致嚴重并發癥和死亡。5歲以下(尤其是2歲以下)的兒童群體發生重癥或有并發癥的風險會明顯增加,6個月以下的兒童死亡率和住院率通常是最高的。
免疫接種是預防流感最重要的公共衛生措施,但并非所有兒童都能接種流感疫苗,或對疫苗產生充分應答。對于無法接種疫苗的兒童、預計對疫苗應答不佳的兒童或沒有時間對疫苗產生應答的兒童,可以將抗病毒藥物化學預防作為免疫接種的輔助手段或替代方法。
凡事都有兩面性,預防用藥同樣可能帶來不少弊端。首先,隨意采取化學預防可能促發抗病毒藥物耐藥,大規模或長期用藥預防流感,可能導致治療重癥或有流感并發癥高風險個體時抗病毒藥物的選擇減少。雖然神經氨酸酶抑制劑耐藥較少見,主要發生于存在長期無癥狀性病毒復制的重度免疫功能受損兒童,但也在健康兒童中出現過。其次,就是不可規避的藥物不良反應。比如,惡心和嘔吐是奧司他韋最常見的不良反應(一日1次服用時發生率為12%)。而除了胃腸道副作用外,有哮鳴或慢性呼吸道疾病病史的患者使用扎那米韋時發生支氣管痙攣的風險也有所增加。除了耐藥率可能增加,巴洛沙韋的其他不良反應包括腹瀉和嘔吐,發生率為2%-6%。
由此可見,應避免對流感采取廣泛或常規的化學藥物預防。對于發生重癥或有并發癥流感風險較高的兒童,可以通過對兒童本人、其家庭接觸者以及家庭外的照料者進行免疫接種來預防流感,該方法優于化學預防。類似于新冠病毒大流行期間推薦的非藥物和行為干預措施,例如避免接觸病患、保持身體距離、佩戴口罩、限制旅行,這些措施也可以幫助降低流感患病率。
化學藥物預防治療包括暴露前和暴露后。
對于發生重癥或有并發癥流感風險非常高且不能接種疫苗也不能采取化學預防的兒童,其3月齡及以上家庭成員或可能與其持續密切接觸的醫務人員如果未接種流感疫苗,可能需采取暴露前預防。一旦在社區中發現流感活動,就應盡快啟動暴露前預防。暴露前預防的持續時間取決于具體適應證。比如,對于在等待流感疫苗產生免疫應答期間接受奧司他韋或扎那米韋化學預防的個體,化學預防應持續至接種流感疫苗后14日。針對其他適應證,應在社區流感活動期間每日使用奧司他韋或扎那米韋進行暴露前化學預防。研究顯示,受試者對長達16周的奧司他韋和扎那米韋方案耐受良好。
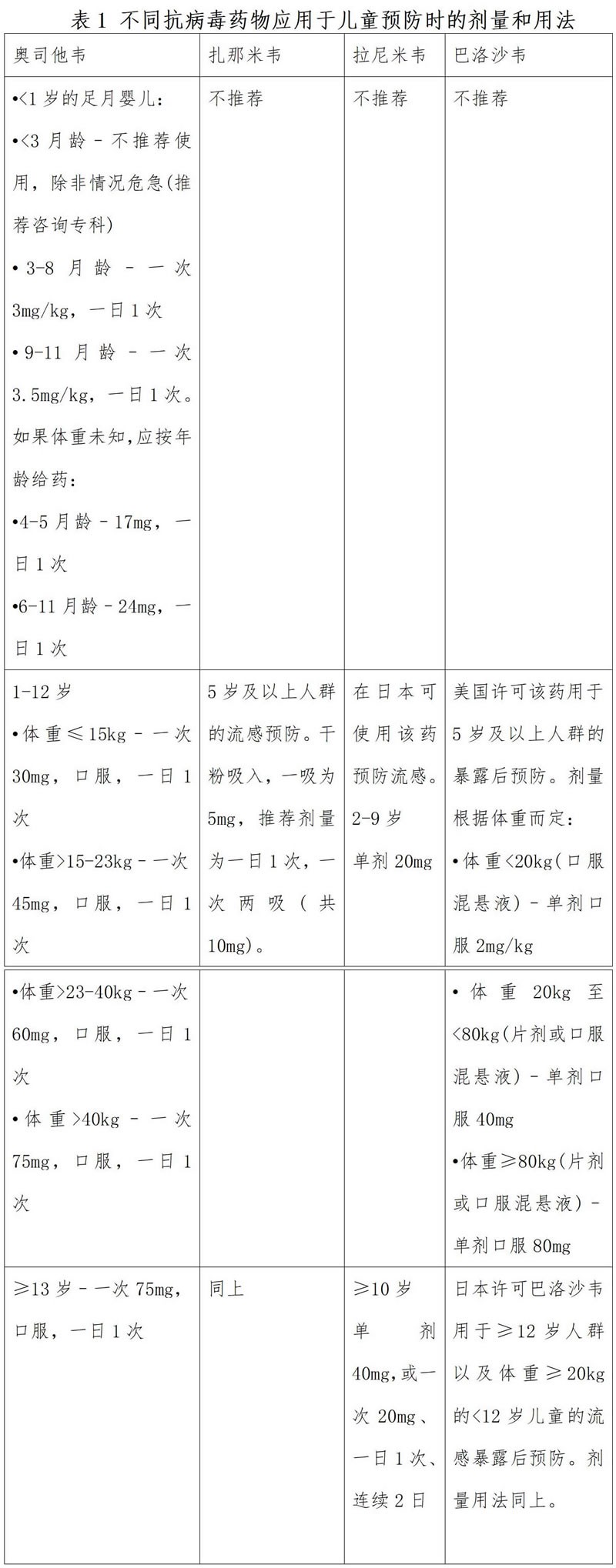
根據最近流感季節的病毒監測和耐藥數據,暴露前預防首選奧司他韋或扎那米韋(針對≥5歲的患者),具體劑量見表1。巴洛沙韋尚未獲批用于暴露前預防。金剛烷類藥物由于耐藥水平較高,不應用于暴露前預防。
對于重度免疫功能受損兒童(如造血干細胞移植受者)的家庭接觸者,如果未接種流感疫苗且≥3月齡,可能需要采取暴露后化學預防。暴露后預防應在暴露后48小時內盡快啟動。暴露后預防的持續時間視具體藥物而定。奧司他韋或扎那米韋應持續使用至最后一次已知暴露后7日。巴洛沙韋應用于暴露后預防(針對≥5歲的患者)時僅需使用單劑藥物。
根據最近流感季節的病毒監測和耐藥數據,兒童暴露后預防首選奧司他韋或扎那米韋(用于≥5歲的兒童)。 巴洛沙韋也可用于≥5歲的兒童。具體劑量見表1。拉尼米韋在日本可用于暴露后預防。帕拉米韋尚未被研究用于預防兒童流感,不適用于化學預防。金剛烷類藥物的耐藥水平較高,不應用于暴露前預防。
綜上,免疫接種是預防兒童流感的主要手段。化學預防并不能消除流感風險。停止化學預防后,會恢復對流感的易感性。具有重癥或有并發癥流感高風險的兒童如果出現流感癥狀應接受醫學評估,從而能夠盡早采取抗病毒治療。
參考文獻:
[1]Influenza: People at higher risk of flu complications. Centers for Disease Control and Prevention. Available at: cdc.gov/flu/highrisk/index.htm
[2]Uyeki TM, Bernstein HH, Bradley JS, et al. Clinical Practice Guidelines by the Infectious Diseases Society of America: 2018 Update on Diagnosis, Treatment, Chemoprophylaxis, and Institutional Outbreak Management of Seasonal Influenzaa. Clin Infect Dis 2019; 68:e1.
[3]US Food and Drug Administration. FDA expands approval of influenza treatment to post-exposure prevention. https://www.fda.gov/news-events/press-announcements/fda-expands-approval-influenza-treatment-post-exposure-prevention (Accessed on November 24, 2020).
[4]American Academy of Pediatrics Committee on Infectious Diseases. Recommendations for prevention and control of influenza in children, 2011-2012. Pediatrics 2011; 128:813.
[5]US Food and Drug Administration. FDA expands approval of influenza treatment to post-exposure prevention. https://www.fda.gov/news-events/press-announcements/fda-expands-approval-influenza-treatment-post-exposure-prevention (Accessed on November 24, 2020).
[6]Heo YA. Baloxavir: First Global Approval. Drugs 2018; 78:693.
[7]Dectova (zanamivir). European Medicines Agency. https://www.ema.europa.eu/en/medicines/human/EPAR/dectova. (Accessed on September 29, 2020).
[8]Relenza (zanamivir inhalation powder). United States Prescribing Information. Revised June, 2018. US Food & Drug Administration. Available at: http://www.accessdata.fda.gov/scripts/cder/drugsatfda/index.cfm (Accessed on March 11, 2019).
[9]Xofluza (baloxavir marboxil) for oral use, prescribing information. https://www.accessdata.fda.gov/drugsatfda_docs/label/2019/210854s001lbl.pdf (Accessed on October 17, 2019).
[10]Kashiwagi S, Watanabe A, Ikematsu H, et al. Long-acting Neuraminidase Inhibitor Laninamivir Octanoate as Post-exposure Prophylaxis for Influenza. Clin Infect Dis 2016; 63:330.
[11]Nakano T, Ishiwada N, Sumitani T, et al. Inhaled Laninamivir Octanoate as Prophylaxis for Influenza in Children. Pediatrics 2016; 138.
[12]Lampejo T. Influenza and antiviral resistance: an overview. Eur J Clin Microbiol Infect Dis 2020; 39:1201.
[13]COMMITTEE ON INFECTIOUS DISEASES; Recommendations for Prevention and Control of Influenza in Children, 2022–2023. Pediatrics October 2022; 150 (4): e2022059274. 10.1542/peds.2022-059274.
[14]López-Medrano F, Alfayate S, Carratalà J, et al. Executive summary. Diagnosis, treatment and prophylaxis of in?uenza virus infection. Consensus statement of the Spanish Society of Infectious Diseases and Clinical Microbiology (SEIMC), the Spanish Society of Pediatric Infectious Diseases (SEIP), the Spanish Association of Vaccinology (AEV), the Spanish Society of Family and Community Medicine (SEMFYC) and the Spanish Society of Preventive Medicine, Public Health and Health Management (SEMPSPGS). An Pediatr (Engl Ed). 2023;98(3):213-227. doi:10.1016/j.anpede.2023.01.012.
[15]Pebody R , Dabrera G , Lackenby A, et al. PHE guidance on use of antiviral agents for the treatment and prophylaxis of seasonal influenza(Version 9.1)[J]. 2019.
北京藥學會 地址:北京市朝陽區北三環中路2號小二樓2層
本網站瀏覽46493266次
Copyright 2012 北京藥學會( 本網站所有內容未經許可,不得以任何形式進行轉載 ) All Rights Reservered