陳 超1 郭代紅1# 薛萬國2劉東杰3 劉皈陽4朱 曼1徐元杰1
(1 解放軍總醫院藥品保障中心/解放軍藥品不良反應監測中心,北京,100853;2 解放軍總醫院信息情報所,北京,100853;3康聯達軟件有限公司,北京,100097;4解放軍第一附屬醫院藥劑藥理科,北京,100037)
摘要:目的 探索計算機輔助篩查藥品不良事件和評估預警技術,旨在彌補現行自發報告模式的不足,改善“被動監測”現狀,使“實時監測”和“預防為主”的藥品風險控制策略成為可能。方法 依托運行良好的軍衛1號醫院信息系統,采用觸發器技術原理,設計開發住院患者藥品不良事件主動監測與評估警示系統,并以臨床藥師人工評估結果為對照,論證系統監測效果。結果 完成了藥物相關性血小板減少、貧血、肝損害、腎損害4個事件的自動識別規則設計,建立了集自動監測、用藥審查、輔助評估、特征分析、高危篩選為一體的關鍵技術路線,開發了配套軟件系統,并對接醫院自發報告監測管理系統,效果驗證陽性預測值達69.4%。結論 本研究建立了醫療機構藥品不良事件“主動監測”與“自愿報告”的聯動工具型平臺,為藥品安全性監測工作的開展提供一種新的思路和實用性的技術工具。
關鍵詞:藥品不良反應、主動監測、重點監測、計算機輔助篩查與評估、臨床藥師
作者簡介:陳超, 女,碩士,解放軍總醫院臨床藥學室,主管藥師, 010-66937146。
通訊作者:郭代紅,女,碩士,主任藥師, 碩士生導師,臨床藥學與藥事管理。guodh301@163.com
我國藥品不良反應(ADR)監測主要采用的是自愿報告系統, 有數據顯示我國 80%的ADR 報告來自醫療機構, 可見醫療機構作為藥品使用環節的主要構成部分已成為藥品安全事件防范、發現與處置的關鍵控制點, 其數據源的質量將直接影響到 ADR 信號的產生和藥物警戒水平[1]。然而,隨著2011年新版《藥品不良反應報告和監測管理辦法》的發布,我國藥品安全風險監管重心已由信息采集轉向技術評估轉移,其中“重點監測”作為法規性文件的新增章節對該項工作的深入開展提出了要求,促使醫療機構的監測現狀面臨諸多挑戰,所以亟需探索和建立新的監測技術方法,利用計算機輔助篩查與評估藥品不良事件(ADE)的自動監測和輔助評估技術可成為解決上述問題的有效手段。
本研究基于良好的醫院信息系統運行環境,設計開發了住院患者藥品不良事件主動監測與評估警示系統(已獲得國家版權局軟件著作權),旨在為藥品安全性監測工作的開展提供一種新的思路和實用性的技術工具,在節省監測資源和提高監測效率的同時,使“實時監測”和“預防為主”的控制策略成為可能。
1 設計思路
1.1建立自動識別、評估警示、高危篩選、自訂制改進為一體的整體構架
通過模擬人工智能,建立邏輯算法,實現計算機輔助篩查-自動識別重點事件,診斷標準不代表監測方案,不良事件的鑒別診斷也通常沒有“金標準”,所以系統的技術方案設計根據實際使用效果預留了自訂制靈活改進的空間。
1.2 自動監測基本理論的選擇
觸發器型藥品不良反應自動識別是目前國外研究較多的一類系統,且通過HIS(Hospital Information System,醫院信息系統)數據集成條件較為成熟,應該優先考慮;而自然語言提取型自動識別技術條件尚不成熟,我國醫學語言編碼處理程序尚待突破;文本信息關鍵詞法自動識別不但取決于不良反應術語與病歷記錄的匹配和對照,而且大部分以特異性不高的臨床癥狀作為主要識別條件,可考慮后期開發。
1.3重點監測事件的選擇
優先選擇4個重要醫學事件“血小板減少”、“貧血”、“肝損傷”、“腎損傷”為切入點,其主要特點是:①具有代表意義、臨床發生率較高、嚴重程度與預后密切相關;②實驗室檢查結果比較穩定,特異性指標相對明確;③具有前期人工監測預試驗基礎[2-5]。
2 系統功能
2.1主動監測后臺伺服程序
主動監測后臺伺服程序是一個運行在數據庫服務器上的軟件,該軟件時刻運行,接受管理員通過【自動監測】模塊下達的計劃指令,為避免數據調取對醫院信息系統主服務器的影響,設定在凌晨啟動,從HIS數據庫中提取數據并按預定規則進行計算處理,最后將結果寫入到【審查評估】ADR數據庫中。次日工作時間,臨床藥師或專業人員即可讀取報警結果,進行相應評估處置。
2.2自動監測模塊
自動監測模塊用來給后臺伺服程序下達指令,監測方式分為兩種:實時監測和回顧分析。回顧分析需要設定監測時段,實時監測設定監測開始時間與監測結束時間,并選擇相關參數,保存后該監測計劃將作為指令轉交后臺伺服程序執行(圖1)。
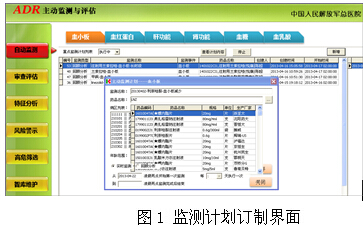
2.3 審查評估模塊
審查評估是提供給臨床藥師或專業人員的輔助決策工具。自動監測結果可按類別分層列表,如評價狀態、審查狀態、報警狀態,由藥師選擇優先順序評估,點擊列表條目,可生成個案評估表。個案評估表盡可能詳細直觀地顯示了患者信息、病生理狀態、醫囑情況、敏感指標變異、不良反應信息、關聯性評價因素列項等。此表中多項指標和列項系統能夠自動測算與標記,輔助專業人員結合患者病歷文本信息或臨床癥狀快速評價。
2.4 特征分析模塊
特征分析模塊是對評價后的大量病歷進行統計分析,獲得發生特征,可針對某個或幾個同類監測計劃進行,系統將自動計算陽性病例、陰性病例、發生率、嚴重程度、危險因素,這些特征性數據有助于明確認知不良事件的發生規律,提示臨床應重點關注的風險人群、可介入的預防時機等。
2.5 風險警示模塊
風險警示模塊分為【干預提示】和【監測報告】兩部分。前者是針對與實時監測計劃產生的“報警”和“審查”異常病歷進行干預處置,可逐一列出“風險點”和“警示原因”,由專業人員查訪患者或查閱詳細信息后判斷是否干預,如不干預,需根據患者實際情況注明理由(有強適應證、透析治療等),如干預,需記錄干預意見(圖2)。后者是針對回顧性研究,如病例對照、橫斷面研究的警示報告模版。
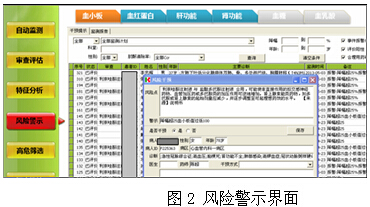
2.6 高危篩選模塊
本模塊設置了目標藥物群-不良事件群的組合監測篩查,可針對院內專科高頻用藥、常用藥物組合或特殊使用、限制使用類藥物進行重點監測和評估,暴露醫院不良事件發生較高的藥品品種、臨床科室、患病人群、藥物治療組合,給醫院加強高風險藥品管理提供警示參考。
2.7 智庫維護模塊
該模塊是本系統的核心字典庫,包括:血小板、血紅蛋白、腎功能、肝功能,在【不良事件配置器】模塊下對不同時間進行詳細的參數配置,設置觸發條件、分級定義等。此外,該模塊還包括了藥品基礎信息、編碼對照、安全用藥審查智庫、權限管理等基礎信息模塊。【安全用藥智庫】審查智庫是底層規則數據庫,即整個用藥審查的規則庫,經過藥學專業人員解讀,翻譯記錄成計算機能夠識別的各類規則,從而實現審查。
3 系統特點
3.1 自動監測結果的輔助快速評估
就ADR自動監測的觸發器原理而言,本身較易實施,自動識別的關鍵在于規則算法,監測效能是否高,但識別信號僅是第一步的基礎性工作。第二步是確認、評價和干預信號,系統可幫助專業人員快速評估、有效分析、干預警示。本研究后期經臨床藥師效果論證顯示,報警結果陽性預測值為69.4%,與國外相關研究0.9%~64%的論證效果相比[6],已達到了較高水平。此外,依據ADE重點監測事件的因果判定的原則,綜合考慮臨床實際的混雜因素,從細節上設計了輔助決策個案評價表。如考慮到“感染”“手術”均可能是“血小板減少”的誘發因素;自動提示患者異常病生理狀態;自動審查用藥問題;自動標記可疑并用藥品;自動計算不良事件特征,幫助專業人員快速評估病例,在系統效果測試中,獲得臨床藥師特別好評。
3.2 基于臨床特征的安全用藥審查自訂制
在評估藥品不良事件之前,應該首先考慮其是否存在用藥問題而增加了風險的發生。目前一些大型合理用藥審查系統已逐步深入臨床應用,在國內以合理用藥監測系統(Prescription Automatic Screening System,PASS)為主[7-9],國外則以醫師處方錄入一用藥決策支持系統(Computerized Physician Order Entry-Clinical Decision Support System,CPOE-CDSS)為主[10-11]。研究發現兩者可一定程度上減少用藥錯誤,然而效用有限,因此類系統主要是“藥物-藥物”審查模式,導致一定量的警示信息與實際臨床情況不符,從而普遍存在警示疲勞問題[12]。此外,大型審查系統通常更新維護不及時,缺乏順應本地調節使用的靈活性和延展性。
本研究的安全用藥審查智庫是在已有合理用藥支持系統運行、PIVAS(pharmacy intravenous admixture service,靜脈用藥集中調配中心)審核、自動化調劑的醫院數字化平臺基礎上,開發能夠自由定制、本地維護和實時更新的審查規則基礎數據庫。此庫可由本單位藥學專業技術人員結合臨床實際,以“患者-藥物”為審查模式,對本單位使用的藥品品種說明書、專業工具書、共識、指南進行再細化翻譯。
3.3 評價風險特征與未知因素以提高“可預防性”
通常評價藥品的風險,要考慮其不良事件發生的嚴重性、發生率、持續時間、靶人群等。本系統可以通過特征分析提供發生率、嚴重程度、不良反應的發生特征,提供路徑分析增加風險的藥物組合,危險因素、這些基本都是在上市前研究未明確的因素,而通過該系統對實際用藥人群的“真實世界研究”,有助于從“不可預防”轉為“可認知”、“可預防”。
3.4 與醫院自發報告系統對接形成聯動監測模式
藥品不良事件主動監測與評估警示系統為醫院開展重點監測提供了工具支持,與醫院藥品不良反應自發報告系統[5](已在86家醫院使用的“軍隊ADR監測管理系統-醫院端”)無縫對接,可直接將主動監測評價為陽性的結果導入ADR自發報告數據庫來進一步篩選信號,也可將自發報告庫篩選的信號導入主動監測系統進行評估驗證,獲得藥品風險實際發生率和群體特征。借此平臺在醫院內部形成常規防控與重點監測相結合的聯動模式。
4 系統應用價值
目前國內將計算機應用于ADR監測領域的研究,主要集中在對ADR自發報告數據庫的信號檢出,而對于結合醫院HIS的ADR自動監測和評估預警技術的研究尚處于探索階段。雖然一些發達國家在該領域的研究已較為深入[13-14],但尚無可套用的系統成品,且不同國家和醫院間HIS系統結構也存在較大差異,標準不同,用藥習慣不同,所以需要結合我國實際制定監測開發方案和配套工具。近年來,隨著我國醫院信息系統的建立和發展,患者的檢查和診療過程已經逐步電子化,為計算機技術監測ADR提供了必備條件。
本研究所研發的系統實現了藥品不良事件的自動識別和輔助評估,設計了自訂制安全用藥審查的規則庫,提供了藥品風險特征及未知因素的數據分析控點,并可與前期開發的醫院ADR自發報告管理系統對接,從而建立醫療機構藥品不良事件主動監測與被動監測的聯動工具型平臺。系統效果驗證表明可有效節省人力、時間、經費等監測資源的投入,擴大監測范圍,提高監測效率,并可實現ADE實時監控與處置,除檢測信號外,還有助于評價信號,并開展流行病學論證研究,具有良好的應用前景。
參考文獻:
[1]陳超,郭代紅,劉皈陽,等.醫療機構藥品不良反應監測的優化實踐[J].中國藥物警戒,2010,7(3):164-168.
[2]ChaoChen,Dai-HongGuo, XiutangCao, et al.Risk factors for thrombocytopenia in adultchinese patients receiving linezolid therapy[J].CURR THER RES CLIN E,2012,73(6):195-206.
[3]陳超,郭代紅,曹秀堂,等.住院患者使用利奈唑胺致相關性血小板減少癥的危險因素分析[J].中國藥物警戒,2012,9(2):71-76.
[4]郭代紅,陳超,李馨,等.6所醫院414例利奈唑胺相關性血小板減少集中監測研究[J].藥物流行病學雜志,2013,22(3):109-113.
[5]陳超,郭代紅,劉皈陽,等. 解放軍藥品不良反應網絡填報管理系統的研發[J].中國藥物應用與監測,2008,5(4):20-24.
[6]Alan J Forster,Alison Jennings,Claire Chow ,et al. A systematic review to evaluate the accuracy of electronic adverse drug event detection[J]. J Am Med Inform Assoc, 2012,19:31-38.
[7]薛萬國.新階段HIS的功能定位與基本特征[J].醫療衛生裝備,2010,31(2):8-10.
[8]俞朝輝,王如華.合理用藥監測軟件在HIS中的應用[J].中國高等醫學教育,2007(4):95-96.
[9]徐帆,朱愷,楊伶俐.利用合理用藥軟件系統對醫院用藥情況進行評價[J].西南國防醫藥,2004,14(3):296-299.
[10]Garg A X, Adhikari N K, McDonald H,et al. Effects of computerized clinical decision support systems on practitioner performance and patient outcomes[J]. JAMA, 2005,293(10):1223-1238.
[11]KhajoueiR, Wierenga P C, Hasman A, et al. Clinicians satisfaction with CP0E ease of use and effect on clinicians' workflow, efficiency and medication safety[J]. Int J Med Inform, 2011, 80(5):297-309.
[12]郭代紅,杜曉曦,陳琿,等. PASS監測用藥風險警示的評估及成因分析[J].中國藥物警戒,2010,7(4):217-220.
[13]Kilbridge P M,Classen D C. Automated surveillance for adverse events in hospitalized patients:back to the future[J]. Qual Saf Health Care,2006,15:148-149.
[14]Andrea L Long, Monica M Horvath, Heidi Cozart. Tailoring adverse drug event surveillance to the paediatric inpatient[J]. Qual Saf Health Care , 2010,19:1-5.
北京藥學會 地址:北京市朝陽區北三環中路2號小二樓2層
本網站瀏覽46593160次
Copyright 2012 北京藥學會( 本網站所有內容未經許可,不得以任何形式進行轉載 ) All Rights Reservered