李新剛,趙志剛*
首都醫科大學附屬北京天壇醫院藥劑科,北京 100050
[摘要] 目的:分析苯妥英與拉莫三嗪致嚴重皮膚不良反應與人類白細胞抗原(humanleucocyte antigen,HLA)-B*1502等位基因的關聯性。方法:計算機檢索截止2013年9月的ISI Web of Knowledge、PUBMED、ScienceDirect、EBSCO、Cochrane、CNKI和萬方數據庫,收集有關苯妥英與拉莫三嗪致嚴重皮膚不良反應與HLA-B*1502等位基因相關性的研究,采用Review Manager 5.2對符合納入標準的研究進行Meta分析。結果:共納入6篇英文研究。Meta分析結果表明,苯妥英和拉莫三嗪的合并OR值分別為5.65 [95% CI: 2.76-11.5]和3.97 [95% CI: 1.36-11.61]。漏斗圖顯示所納入的研究未見明顯的發表偏倚。結論:HLA-B*1502等位基因與苯妥英和拉莫三嗪致嚴重皮膚不良反應間存在明顯的相關性。
[關鍵詞] 苯妥英;拉莫三嗪;HLA-B*1502;Meta分析
A Meta-analysis on the Association between HLA-B*1502 and Phenytoin or Lamotrigine induced Severe Cutaneous Adverse Drug Reaction
LI Xin-gang, ZHAO Zhi-gang*
Department of pharmacy, Beijing Tiantan Hospital Affiliated to Capital Medical University, Beijing 100050, China
[Abstract] Objective: To analyze the effects of humanleucocyte antigen (HLA)-B*1502 on phenytoin and lamotrigine induced severe cutaneous adverse drug reaction. Methods: ISI Web of Knowledge、PUBMED、ScienceDirect、EBSCO、Cochrane、CNKI and wanfang data were searched for the literature published before September 2013. Meta-analysis were performed by Review Manager 5.2 software. Results: 6 English studies were included finally. Meta-analysis showed that OR of phenytoin and lamotrigine were 5.65 [95% CI: 2.76-11.5] and 3.97 [95% CI: 1.36-11.61], respectively. Funnel plot analysis showed symmetry, indicting less possible publication bias and the result was partly reliable. Conclusion: There is a significant association between HLA-B*1502 and phenytoin and lamotrigine-induced severe cutaneous adverse drug reaction.
[Keywords] phenytoin; lamotrigine; HLA-B*1502; Meta-analysis
人類白細胞抗原(humanleucocyte antigen,HLA)位于人類染色體6p21.3,是一群緊密連鎖有復等位基因,包括100余個基因座共有554個等位基因,全長3600kb,是調控人體特異性免疫應答和決定疾病易感性個體差異的主要基因系統,在種族間和同族的不同群體間具有明顯的特異性[1]。HLA-B*1502是HLA基因B位點的一個基因亞型,幾乎只存在于亞洲人種之中,其中中國漢族人(包括臺灣地區)、菲律賓人、馬來西來人和泰國人的攜帶率估計在10%~15%之間,包括印度人在內的南亞人群攜帶者約為2%~4%,而在日本和韓國人群中的攜帶者極少。2007年12月12日,美國食品藥品監督管理局(Food and Drug Administration,FDA)向醫務人員提出警示:卡馬西平會增加HLA-B*1502陽性亞裔患者出現Stevens-Johnson綜合癥(Stevens-Johnson syndrome,SJS)和中毒性表皮壞死松解癥(toxic epidermal necrolysis,TEN)出現的風險,因此應避免將卡馬西平應用于此類患者,除非效益明顯大于風險,相關信息已寫入卡馬西平的說明書中。2008年11月24日,FDA又發布消息稱,他們正在調查關于苯妥英(phenytoin,PHT)用于HLA-B*1502等位基因陽性患者亞裔患者治療出現JSJ/TEN的初步數據[2]。此外還有多項研究發現:HLA-B*1502等位基因與拉莫三嗪(lamotrigine,LTG)致SJS/TEN可能存在一定的相關性[3-7],但尚未得到一致結論。此次系統評價對已有研究進行Meta分析,綜合以往研究結果,希望更準確的評價PHT和LTG致SJS/TEN與HLA-B*1502等位基因的相關性。
1 資料與方法
1.1 文獻檢索
計算機檢索截止2013年9月的ISI Web of Knowledge、PUBMED、ScienceDirect、EBSCO、Cochrane、CNKI和萬方數據庫,查找HLA-B*1502與苯妥英和拉莫三嗪致SJS/TEN相關性的原始研究。檢索策略采用包括“抗癲癇藥物(antiepileptic drugs)”或“苯妥英(phenytoin)”或“拉莫三嗪(lamotrigine)”和“HLA”或“HLA-B*1502”或“人白細胞抗原(humanleucocyte antigen)”等相關中英文文獻檢索詞進行檢索,只檢索以中文或英文發表的相關文獻。此外,對納入文獻的參考文獻進行閱讀以補充檢索。
1.2 納入與排除標準
納入Meta分析的研究必須滿足如下標準:①研究中同時設有不良反應組與對照組;②研究納入的患者均為癲癇病人;③確定嚴重的皮膚不良反應是由患者使用苯妥英或拉莫三嗪導致;④所有患者全部進行HLA-B*1502檢測。符合以下任意一條或多條標準的均須排除于Meta分析之外:①患者同時服用多種抗癲癇藥物引起的嚴重皮膚不良反應;②樣本量小于3名患者;③只有摘要的文獻;④數據不完整的文獻;⑤重復報告的文獻。由兩名評價人員獨立通過瀏覽題目,摘要選擇相關文獻,然后查找出相關文獻全文,閱讀全文,依據納入與排除標準對文獻進行評價,選擇相符的文獻。按預先制定的資料提取表提取相關數據,所有數據均由非提取人員進行核查以確保準確。對存在爭議的文獻可通過討論或咨詢第三位評價人員的意見進行裁定。
1.3 統計分析方法
采用Review Manager 5.2軟件進行Meta分析,采用比值比(odds ratio, OR)及其95%置信區間(confidence interval,CI)為效應指標來比較,檢驗水平為P = 0.05,P < 0.05則認為組間存在顯著差異,否則為無統計學差異。在分析過程中采用χ2檢驗來評價納入研究的異質性,若異質性檢驗結果為P > 0.1,說明多個研究間具有同質性,采用固定效應模型;反之則說明研究間不具有同質性,首先進行異質性分析和處理,若仍無法消除異質的資料,可采用隨機效應模型。
2 結果
2.1 納入研究的基本情況
依入排標準最終納入6篇文獻[3-8],涉及9項對照研究和468名癲癇患者,具體檢索流程見圖1。納入文獻的發表時間為2007至2013年,除Locharemkul的研究人群為泰國人外,其余研究對象均為中國漢族人群或后裔。苯妥英致嚴重皮膚不良反應與HLA-B*1502等位基因的關聯性有4項研究,不良反應組46例,對照組246例;拉莫三秦致嚴重皮膚不良反應與HLA-B*1502等位基因的關聯性有5項研究,不良反應組19例,對照組157例。
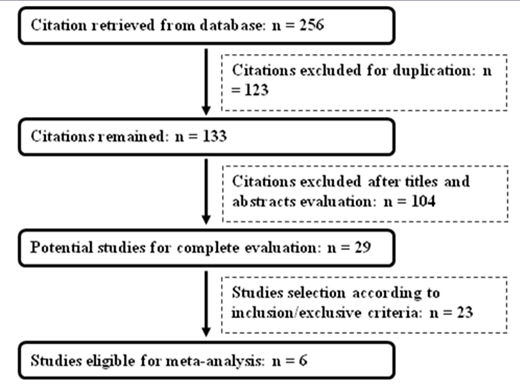
圖1 納入文獻的篩選流程圖
Fig. 1 Identification of eligible studies
2.2 HLA-B*1502等位基因與苯妥英致嚴重皮膚不良反應關聯性Meta分析
納入4項研究,依Review Manager 5.2軟件的要求輸入研究及數據,Meta分析的森林圖見圖2。異質性檢驗顯示P = 0.47,表明各個研究間具有同質性,可以采用固定效應模型法進行分析。SJS/TEN組納入46例患者,其中20例攜帶有HLA-B*1502基因,對照組246例患者中34為HLA-B*1502陽性。合并OR(95% CI)為5.65 [2.76 ~ 11.57],總體效應檢測P < 0.00001,表明HLA-B*1502等位基因與苯妥英致嚴重皮膚不良反應間具有很強的相關性。
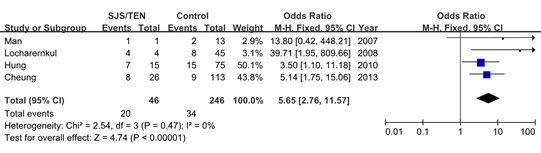
圖 2 HLA-B*1502等位基因與苯妥英致SJS/TEN間關系的Meta分析森林圖
Fig. 2 Forest plot of meta-analysis for association between HLA-B*1502 and Phenytoin-induced SJS/TEN
2.3 HLA-B*1502等位基因與拉莫三嗪致嚴重皮膚不良反應關聯性Meta分析
有5項研究最終納入了Meta分析,SJS/TEN組19例患者中6例是HLA-B*1502基因攜帶者,對照組的157名患者中有16人攜帶HLA-B*1502等位基因。各研究間具有較好的同質性(P = 0.85),因此采用固定效應模型法進行分析。合并OR(95% CI)為3.97 [1.36 ~ 11.61],總體效應檢測P = 0.01,表明HLA-B*1502等位基因與拉莫三嗪致嚴重皮膚不良反應間具有顯著的相關性。
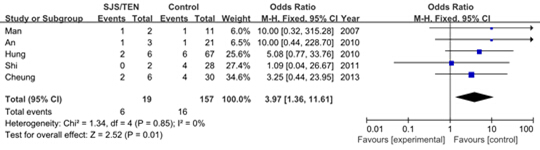
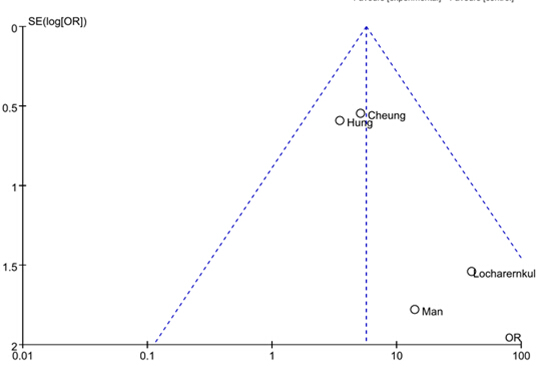
圖 3 HLA-B*1502等位基因與拉莫三嗪致SJS/TEN間關系的Meta分析森林圖
Fig. 3 Forest plot of meta-analysis for association between HLA-B*1502 and lamotrigine-induced SJS/TEN
2.4 發表偏倚評估
應用Review Manager 5.2軟件對納入研究進行發表偏倚分析,結果見圖4和圖5。兩研究的漏斗圖基本對稱,表明分析中不存在發表偏倚。
圖4 HLA-B*1502與苯妥英致SJS/TEN相關性Meta分析的漏斗圖
Fig. 4 Funnel plot for publication bias in meta-analysis of association of HLA-B*1502 and phenytoin-induced SJS/TEN
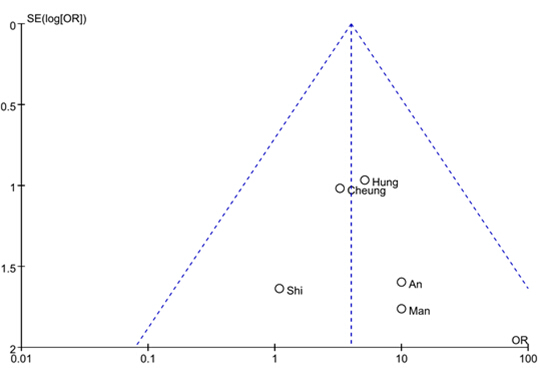
圖5 HLA-B*1502與拉莫三嗪致SJS/TEN相關性Meta分析的漏斗圖
Fig. 5 Funnel plot for publication bias in meta-analysis of association of HLA-B*1502 and lamotrigine-induced SJS/TEN
3 討論
苯妥英、拉莫三嗪、磷苯妥英與卡馬西平均屬于芳香類抗癲癇藥物,其中卡馬西平致SJS/TEN與HLA-B*1502的相關性已得到了確認,且相關警示已寫入藥品說明書中。雖然已有文獻報道,但其它幾個藥物致SJS/TEN與HLA-B*1502等位基因的關系仍未得到明確[3-8]。本研究Meta分析顯示:HLA-B*1502等位基因與苯妥英和拉莫三嗪致SJS/TEN有顯著的相關性。磷苯妥英是苯妥英的前體藥物,在體內轉化為苯妥英后發揮抗癲癇作用,故而關于苯妥英的任何風險磷苯妥英同樣存在[2]。從研究數據中我們可以看到,不是所有出現SJS/TEN的患者均為HLA-B*1502等位基因攜帶者,也并不是所有HLA-B*1502等位基因攜帶者均會發生SJS/TEN,這說明SJS/TEN的發生還有其它因素有關。
抗癲癇藥物引發SJS/TEN的機制尚不清楚,除了與基因多態性因素有關外,也可能存在免疫學方面的因素。有學者發現卡馬西平與HLA-B*1502結合的多肽間以非共價鍵結合,從而引起了SJS/TEN患者細胞毒性T細胞反應[9]。研究者還發現患者對卡馬西平、苯妥英或拉莫三嗪過敏時,藥物特異性T細胞大量表達Vβ5.1細胞受體,這表明Vβ5.1可能在藥物的致敏反應中發揮重要作用[10-12]。
在解釋基因型與藥物不良反應之間的關系時應該非常謹慎,隨著研究的不斷深入,會有更多的基因被發現,多種基因可能與藥物的不良反應相關。以卡馬西平為例,除了已經明確的HLA-B*1502外,HLA-B*3101[13]、HLA-B*5801和HLA-B*4001[7]等位基因均可能與卡馬西平致SJS/TEN存在相關性。如何排除其它基因的影響,單獨研究特定基因與藥物致敏之間的關系,可能會成為此類研究的發展方向。除基因因素外,還有許多非遺傳因素可能會使藥物產生致SJS/TEN,但受限于納入研究信息量的不足,不能對這些因素一一考察。此外,本次Meta分析中納入的研究沒有統一的試驗設計方案,符合標準的文獻僅有幾篇、納入的病例數較少、苯妥英和拉莫三嗪的給藥劑量和用藥時間也不完全相同,這些都會使本次系統評價的結果產生一定的偏倚。
4 結語
綜上所述,HLA-B*1502等位基因與苯妥英和拉莫三嗪致嚴重皮膚不良反應顯著相關,但藥物致嚴重皮膚不良反應還受到了多種其它基因的影響,仍需要大樣本高質量的前瞻性研究來確認。
參考文獻
[1] 石奕武. 芳香族抗癲癇藥物導致皮膚型藥物不良反應與HLA基因的關系進展[J]. 實用醫學雜志, 2012, 28(13): 2119-2121.
[2] 美國警示攜帶HLA-B*1502等位基因的患者使用苯妥英可能導致嚴重皮膚反應[J]. 中國藥物警戒, 2009, 6(2): 122-123.
[3] An DM, Wu XT, Hu FY, Yan B, Stefan H, Zhou D. Association study of lamotrigine-induced cutaneous adverse reactions and HLA-B*1502 in a Han Chinese population[J]. Epilepsy Res. 2010, 92(2-3):226-230.
[4] Shi YW, Min FL, Liu XR, Zan LX, Gao MM, Yu MJ, Liao WP. Hla-B alleles and lamotrigine-induced cutaneous adverse drug reactions in the Han Chinese population[J]. Basic Clin Pharmacol Toxicol. 2011, 109(1): 42-46.
[5] Man CB, Kwan P, Baum L, Yu E, Lau KM, Cheng AS, Ng MH. Association between HLA-B*1502 allele and antiepileptic drug-induced cutaneous reactions in Han Chinese[J]. Epilepsia. 2007, 48(5): 1015-8.
[6] Hung SI, Chung WH, Liu ZS, Chen CH, Hsih MS, Hui RC, Chu CY, Chen YT. Common risk allele in aromatic antiepileptic-drug induced Stevens-Johnson syndrome and toxic epidermal necrolysis in Han Chinese[J]. Pharmacogenomics. 2010, 11(3):349-356.
[7] Cheung YK, Cheng SH, Chan EJ, Lo SV, Ng MH, Kwan P. HLA-B alleles associated with severe cutaneous reactions to antiepileptic drugs in Han Chinese[J]. Epilepsia. 2013, 54(7): 1307-1314.
[8] Locharernkul C, Loplumlert J, Limotai C, Korkij W, Desudchit T, Tongkobpetch S, Kangwanshiratada O, Hirankarn N, Suphapeetiporn K, Shotelersuk V. Carbamazepine and phenytoin induced Stevens-Johnson syndrome is associated with HLA-B*1502 allele in Thai population[J]. Epilepsia. 2008, 49(12): 2087-91.
[9] Yang CW,Hung SI,Juo CG, Lin YP, Fang WH, Lu IH, Chen ST, Chen YT. HLA-B*1502-bound peptides: implications for the pathogenesis of carbamazepine-induced Stevens-Johnson syndrome[J]. J Allergy Clin Immunol, 2007, 120(40): 870-877.
[10] Naisbitt DJ, Britschgi M, Wong G, Farrell J, Depta JP, Chadwick DW, Pichler WJ, Pirmohamed M, Park BK. Hypersensitivity reactions to carbamazepine: characterization of the specificity, phenotype, and cytokine profile of drug specific T cell clones[J]. Mol Pharmacol, 2003, 63(3): 732-741.
[11] Hashizume H,Takigawa M,Tokura Y. Characterization of drug-specific T cells in phenobarbital-induced eruption[J]. J Immunol, 2002, 168(10): 5359-5368.
[12] Naisbitt DJ,Farrell J,Wong G,Depta JP, Dodd CC, Hopkins JE, Gibney CA, Chadwick DW, Pichler WJ, Pirmohamed M, Park BK. Characterization of drug-specific T cells in lamotrigine hypersensitivity[J]. J Allergy Clin Immunol, 2003, 111(6): 1393-1403.
[13] Thorn CF, Leckband SG, Kelsoe J, Leeder JS, Müller DJ, Klein TE, Altman RB. PharmGKB summary: carbamazepine pathway[J]. Pharmacogenet Genomics. 2011, 21(12):906-910
北京藥學會 地址:北京市朝陽區北三環中路2號小二樓2層
本網站瀏覽46592906次
Copyright 2012 北京藥學會( 本網站所有內容未經許可,不得以任何形式進行轉載 ) All Rights Reservered